Tevimbra(Tislelizumab-jsgr)的說明書
一、名稱:Tislelizumab-jsgr
商品名稱:Tevimbra
二、適應症:
Tevimbra(Tislelizumab-jsgr)作為一種單一藥物,適用於治療之前進行了不含PD-(L)1抑製劑的全身化療的不可切除或轉移性食管鱗狀細胞癌(ESCC)成年患者。
三、用法用量:
1、推薦劑量:Tevimbra的推薦劑量為200mg,每3周靜脈注射一次,直至疾病進展或出現不可接受的毒性。在60分鐘內進行第一次輸液。如果耐受,隨後的輸注可以在30分鐘內進行。
2、劑量調整:不建議減少Tevimbra的劑量。一般來說,對於嚴重(3級)免疫介導的不良反應,應扣留Tevimbra。對於危及生命(4級)的免疫介導不良反應、需要全身免疫抑制治療的複發性嚴重(3級)免疫介導反應,或在開始使用類固醇後12週內無法將皮質類固醇劑量減少到每天10mg或更少的潑尼松當量,應永久停用Tevimbra。
四、不良反應:
在Tevimbra的治療食管鱗狀細胞癌的臨床研究中,最常見的(≥20%)不良反應(包括實驗室異常)包括血糖升高、血紅蛋白降低、淋巴細胞減少、鈉減少、白蛋白減少、鹼性磷酸酶升高、貧血、疲勞、天門冬氨酸轉氨酶(AST)升高、肌肉骨骼疼痛、體重下降、丙氨酸氨基轉移酶(ALT)升高和咳嗽;經上市後,還出現了皮膚和皮下組織疾病等不良事件,包括史蒂文斯-約翰遜綜合徵、中毒性表皮壞死松解症(包括致命病例)。 xa0
五、供應和儲存:
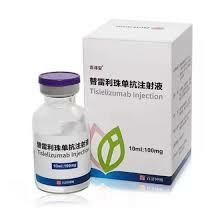
Tevimbra注射液是一種清澈至微乳白色、無色至微黃色的溶液,裝在一個裝有100mg/10mL(10mg/mL)單劑量小瓶的紙箱中;存放在原紙箱中的2°C至8°C(36°F至46°F)冰箱中,以避免光照。不要凍結。不要搖晃。
六、特殊人群:
根據其作用機制,孕婦使用Tevimbra會對胎兒造成傷害。因此建議有生殖能力的女性在使用Tevimbra治療期間以及在最後一劑給藥 後的4個月內使用有效的避孕措施;建議婦女在治療期間以及在最後一劑給藥後的4個月內不要進行母乳喂養。
七、作用機制:
PD-1配體PD-L1和PD-L2與T細胞上發現的PD-1受體結合,抑制T細胞增殖和細胞因子產生。 PD-1配體的上調出現在一些腫瘤中,並且通過該途徑的信號傳導可有助於抑制腫瘤的活性T細胞免疫監視。 Tevimbra的主要成分Tislelizumab-jsgr通過結合PD-1並阻斷其與PD-L1和PD-L2的相互作用,釋放PD-1途徑介導的免疫反應抑制,包括抗腫瘤免疫反應。 Tislelizumab-jsgr降低異種移植模型和人類PD-1轉基因小鼠模型中的腫瘤生長。
參考資料:https://dailymed.nlm.nih.gov/dailymed/drugInfo.cfm?setid=08ef1e3e-496f-4b0b-94ee-fbba3cc1985a##
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
.jpeg)


















