2025年關於Avtozma(tocilizumab-anoh)的最新新聞消息
美國食品藥品監督管理局(FDA)已批准Avtozma(tocilizumab-anoh)作為Actemra(tocilizumab)的生物類似物,提供靜脈(IV)和皮下(SC)兩種劑型。 Avtozma原名CT-P47,是一種白細胞介素-6受體拮抗劑,適用於多種病症的治療,包括中度至重度活動性類風濕性關節炎、成人鉅細胞動脈炎、2歲及以上患有活動性多關節幼年特發性關節炎或系統性幼年特發性關節炎的患者,以及需要補充氧氣或機械通氣的新冠肺炎住院成年患者。
該批准的基礎是經過科學證據綜合審查,證明Avtozma與Actemra之間高度相似。這包括一項III期研究的數據,該研究評估了tocilizumab-anoh與參考藥物tocilizumab(r-TCZ)在471名中度至重度活動性類風濕性關節炎患者中的療效和安全性。
在研究的第一個治療階段,參與者被隨機分為兩組,接受託珠單抗-anoh或r-TCZ靜脈注射,持續到第20週。在第24週之前的第二個階段中,接受r-TCZ的患者再次隨機分組,要么繼續使用該藥物,要么切換到tocilizumab-anoh,直到第48週。共同主要終點是在第12周和第24週時使用紅細胞沉降率(DAS28-ESR)評估疾病活動評分的變化。
結果顯示,在第12周和第24週,DAS28-ESR的估計治療差異分別為-0.01和-0.10,表明兩者之間的治療效果相近。此外,Avtozma與參考產品在藥代動力學、安全性和免疫原性方面也表現出可比性,且從r-TCZ切換到Avtozma時,持續的療效沒有安全性問題。
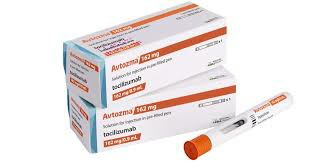
Avtozma提供不含防腐劑的溶液,包裝形式包括20mg/mL的單劑量小瓶(80mg/4mL、200mg/10mL、400mg/20mL)用於靜脈輸注,以及162mg/0.9mL的單劑量預充式註射器和自動注射器用於皮下注射。這一批准為患者提供了更多靈活的治療選擇。
參考資料:https://www.rheumatologyadvisor.com/news/fda-approves-tocilizumab-biosimilar-avtozma/
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
.jpeg)


















