恩西地平enasidenib說明書
一. 全部名稱:恩西地平,Idhifa,Enasidenib
通用名稱:恩西地平
商品名:Idhifa
二. 適應症和用法
恩西地平是一種異檸檬酸脫氫酶2抑製劑,用於治療經FDA批准的試驗檢測到異檸檬酸脫氫酶2 (IDH2)突變的複發性或難治性急性髓細胞白血病(AML)成年患者.
三.劑量和用法
每日一次口服100 mg,直至疾病惡化或出現不可接受的毒性.對於沒有疾病進展或不可接受的毒性的患者,至少治療6個月,以留出臨床反應時間。
四.劑型和強度
藥片:50毫克或100毫克
五. 禁忌症
無
六.警告和注意事項
1.在臨床試驗中,14%接受恩西地平治療的患者出現了分化綜合徵,如果不治療,可能會危及生命或致命。分化綜合徵與骨髓細胞的快速增殖和分化有關。雖然沒有鑑別綜合徵的診斷測試,但接受恩西地平治療的患者的症狀包括急性呼吸窘迫,表現為呼吸困難或缺氧(68%)以及需要補充氧氣(76%);肺部浸潤(73%)和胸腔積液(45%);腎功能損害(70%);發熱(36%);淋巴結病(33%);骨痛(27%);體重快速增加的外周水腫(21%);和心包積液(18%)。還觀察到肝、腎和多器官功能障礙。在恩西地平開始後1天至5個月內,觀察到伴有或不伴有高白細胞增多的分化綜合徵。如果懷疑有分化綜合徵,開始口服或靜脈注射皮質類固醇(如每12小時10 mg地塞米松)並監測血流動力學,直至症狀改善。僅在症狀緩解後才逐漸減少皮質類固醇。過早停止皮質類固醇治療可能會導致分化綜合徵症狀復發。如果需要插管或呼吸機支持的嚴重肺部症狀或腎功能不全在開始使用皮質類固醇後持續超過48小時,則中斷恩西地平,直到體徵和症狀不再嚴重。建議住院密切觀察和監測有肺部和/或腎臟表現的患者。
2.胚胎-胎兒毒性。基於動物胚胎-胎兒毒性研究,當給孕婦使用時,恩西地平可導致胚胎-胎兒損傷。在動物胚胎-胎兒毒性研究中,根據推薦的人體劑量下的濃度-時間曲線下面積(AUC ),恩西地平引起的胚胎-胎兒毒性始於穩態臨床暴露量的0.1倍。告知孕婦對胎兒的潛在風險。建議具有生殖潛力的女性在使用恩西地平治療期間以及最後一次給藥後至少2個月內使用有效的避孕措施。建議有生殖能力的女性伴侶的男性在使用恩西地平恩西地平治療期間以及在最後一次給藥後至少2個月內使用有效的避孕措施。
七.不良反應
最常見的不良反應(≥20%)是噁心、嘔吐、腹瀉、膽紅素升高和食慾下降。
八.藥物相互作用
xa01.恩西地平對其他藥物的影響
OATP1B1、OATP1B3和BCRP底物
恩西地平是一種OATP1B1、OATP1B3和BCRP抑製劑。與恩西地平合用會增加OATP1B1、OATP1B3和BCRP底物的暴露,這可能會增加這些底物不良反應的發生率和嚴重性。 根據相應處方信息中的建議和臨床指徵,減少OATP1B1、OATP1B3和BCRP底物的劑量。
2.某些P-糖蛋白底物
恩西地平是一種P-gp抑製劑。與恩西地平合用增加了P-gp底物的暴露,這可能會增加這些底物不良反應的發生率和嚴重性.對於小濃度變化可能導致嚴重不良反應的P-gp底物,減少劑量或修改此類P-gp底物的給藥頻率,並按照相應處方信息中的建議監測不良反應。
九.在特定人群中使用
1.懷孕。 可能會對胎兒造成傷害。在開始恩西地平治療前確認懷孕狀態。如果在懷孕期間使用,或者如果患者或其伴侶在治療期間懷孕,告知患者潛在的胎兒危險。
2.哺乳。 不知道恩西地平是否分佈在乳汁中。治療期間和停藥後≥2個月停止護理。
3.具有生殖潛力的女性和男性。 具有生殖能力的女性和作為此類女性伴侶的男性在接受藥物治療期間以及停藥後≥2個月內應採用適當的避孕方法。動物研究表明,恩西地平可能會損害女性和男性的生育能力。
4.老年人使用與年輕人相比,安全性和有效性總體上沒有差異。
5.肝臟損傷。 在人群藥代動力學分析中,輕度肝損傷不會改變全身暴露。 但,暴露量可能會增加,因為恩西地平主要通過肝臟代謝。
6.腎臟損傷。 在群體藥代動力學分析中,腎功能損害不會改變全身暴露。
十.描述
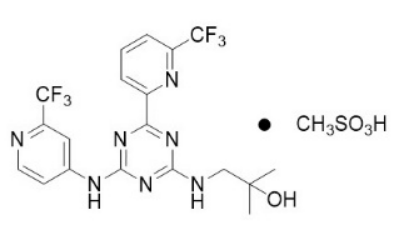
恩西地平是異檸檬酸脫氫酶-2 (IDH2)酶的抑製劑。依那普利可以作為甲磺酸鹽獲得,化學名為:2-甲基-1-[(4-[6-(三氟甲基)吡啶-2-基]-6-{[2-(三氟甲基)吡啶-4-基]氨基}-1,3,5-三嗪-2-基)氨基]丙-2-醇甲磺酸鹽。
化學結構是:
十一.臨床藥理學
1.作用機制
恩西地平是一種異檸檬酸脫氫酶2 (IDH2)酶的小分子抑製劑。在體外,恩西地平以比野生型酶低約40倍的濃度靶向突變體IDH2變體R140Q、R172S和R172K。在IDH2突變的AML小鼠異種移植模型中,恩西地平抑制突變的IDH2酶導致2-羥基戊二酸(2-HG)水平降低,並在體外和體內誘導骨髓分化。在IDH2突變的AML患者的血液樣本中,恩西地平降低了2-HG水平,減少了原始細胞計數,增加了成熟髓樣細胞的百分比。
2.藥代動力學
血漿濃度峰值(C最大)在單劑量100毫克後為1.4微克/毫升[變異係數(CV % 50%],在穩定狀態下每日100毫克為13.1微克/毫升(CV% 45%)。恩西地平的濃度-時間曲線下面積(AUC)以近似劑量比例的方式從50 mg(批准的推薦劑量的0.5倍)增加到450 mg(批准的推薦劑量的4.5倍)。每日一次給藥後29天內達到穩態血漿水平。當每天給藥一次時,蓄積約為10倍。
3.吸收
口服100 mg劑量的恩西地平後,絕對生物利用度約為57%。單劑量口服後,達到C的中位時間最大(T最大)是4個小時。
4.分配
恩西地平的平均分佈體積(Vd)為55.8升(CV% 29)。在體外,恩西地平的人血漿蛋白結合率為98.5%,其代謝物AGI-16903的結合率為96.6%。
5.淘汰
恩西地平的終末半衰期為7.9天,平均全身清除率(CL/F)為0.70升/小時(CV% 62.5)。
6.新陳代謝
恩西地平佔循環中放射性的89 %, AGI-16903,N-脫烷基代謝物,佔循環中放射性的10%。
體外恩西地平的代謝由多種細胞色素P450 (CYP)酶(例如,CYP1A2、CYP2B6、CYP2C8、CYP2C9、CYP2C19、CYP2D6和CYP3A4)和多種UDP葡萄醣醛酸轉移酶(UGT)(例如,UGT1A1、UGT1A3、UGT1A4、UGT1A9、UGT2B7和UGT2B15)介導。代謝物AGI-16903的進一步代謝也由多種酶(例如,CYP1A2、CYP2C19、CYP3A4、UGT1A1、UGT1A3和UGT1A9)在體外介導。
7.排泄
百分之八十九(89%)的恩西地平在糞便中消除,在尿液中消除11%。糞便中未改變的恩西地平的排泄量佔放射性標記藥物的34%,在尿液中佔0.4%。
8.特定人群
在以下協變量中,未觀察到對恩西地平藥代動力學有臨床意義的影響:年齡(19歲至100歲)、種族(白人、黑人或亞裔)、輕度肝功能損害[定義為總膽紅素≤正常值上限(ULN)和天冬氨酸轉氨酶(AST) >ULN或總膽紅素1至1.5倍ULN和任何AST]、腎功能損害(科克羅夫特-高爾特公式定義為肌酐清除率≥30 mL/min)、性別、體重(39 kg至136 kg)和體表面積。
9.藥物相互作用研究
臨床研究
OATP1B1、OATP1B3和BCRP底物:多劑量IDHIFA 100 mg後合用瑞舒伐他汀10 mg可增加瑞舒伐他汀C最大366%和AUC0-INF上升了244%。
P-gp底物:在多劑量IDHIFA 100 mg後合用地高辛0.25 mg增加了地高辛C最大26%和AUC0-30小時下降了20%。
孟加拉齊斯卡製藥零售價格50mg60粒4千元左右,孟加拉珠峰製藥零售價格50mg30粒5千元左右,老撾盧修斯製藥零售價格2千元左右,都有政府批文,患者可根據自身經濟情況選擇藥物版本。 如果想獲取更多優質信息可以聯繫藥得,藥得會盡全力為您了解到更多海外優質藥物。
xa0
xa0
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
.jpeg)


















