佩米替尼(Pemigatinib)療效與價格深度解析:從最新熱點到患者關切
一、熱點引入:肝膽腫瘤新藥的聚焦
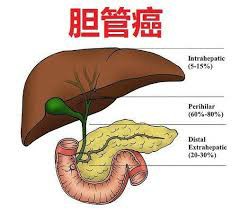
近年來,腫瘤靶向治療的賽道不斷擴展,特別是在膽管癌(Cholangiocarcinoma)等罕見但惡性程度極高的腫瘤領域。 2024年,美國臨床腫瘤學會(ASCO)會議上,針對FGFR2融合或重排陽性的晚期膽管癌的靶向治療數據再度成為學界關注的焦點。其中,佩米替尼(Pemigatinib)作為FDA首批批准的針對FGFR2基因異常的口服靶向藥,被稱為“膽管癌患者的新希望”。
就在今年,多項真實世界研究也在國內外陸續公佈,顯示佩米替尼在不同線次治療中均有較好的療效和耐受性。隨著越來越多的患者與醫生開始接觸這一新藥,其療效與價格也逐漸成為患者群體討論的熱點。
本文將系統解析佩米替尼的臨床療效、適應症拓展進展,並結合國內外價格對比,幫助患者全面了解這款藥物。

二、什麼是佩米替尼?作用機制解析
佩米替尼(Pemigatinib)是一款口服小分子選擇性FGFR抑製劑,主要靶向FGFR1、FGFR2和FGFR3。
1.靶點機制:FGFR基因突變或融合重排會導致細胞信號通路異常激活,促進腫瘤發生髮展。佩米替尼通過抑制FGFR的磷酸化過程,阻斷其下游信號通路,從而抑制癌細胞的生長和擴散。
2.批准進展:2020年,FDA首次批准佩米替尼用於治療既往接受過至少一次系統治療的、存在FGFR2融合或重排的局部晚期或轉移性膽管癌患者。這是膽管癌領域首個FGFR靶向藥物。
3.研究拓展:目前,佩米替尼還在探索用於骨髓增生異常綜合徵(MDS)、尿路上皮癌等疾病的可能性,顯示出更廣泛的臨床前景。
三、佩米替尼的臨床療效
在國際多項臨床研究中,佩米替尼均展現出較強的療效。
1.FIGHT-202研究(關鍵性試驗)
入組對象:FGFR2融合或重排陽性的膽管癌患者
主要結果:
客觀緩解率(ORR):36%
疾病控制率(DCR):82%
中位無進展生存期(PFS):6.9個月
中位總生存期(OS):21.1個月
結論:相較於傳統化療(ORR不足10%),佩米替尼顯著改善了患者的緩解率和生存期。
2.真實世界應用
國內外的多中心臨床實踐表明,即便在二線或三線用藥中,佩米替尼依然能為部分患者帶來持久的緩解。
部分患者甚至在用藥後腫瘤明顯縮小,症狀顯著改善,生活質量得到提升。
3.安全性
常見副作用包括高磷血症、口腔潰瘍、指甲變化、皮疹及輕中度消化道反應。
大多數不良事件為可控和可逆,不會導致嚴重停藥。
四、國內外價格差異與購買渠道
儘管療效令人期待,但價格始終是患者最關注的現實問題。
1.國內市場情況
佩米替尼已在國內上市,名為“佩米替尼片”。
尚未進入醫保目錄,因此患者需自費購買。
市場上常見規格:
4.5mg × 14片
9mg × 14片
國內價格區間:2萬–5萬元/盒(因規格和渠道不同略有差異)。
2.海外市場情況
在美國、歐洲,常見規格為 13.5mg × 14片。
售價:約 7萬元人民幣/盒(價格隨匯率波動)。
3.仿製藥選擇
以老撾盧修斯製藥(Lucius)生產的仿製版為例:
規格:4.5mg × 14片
售價:700元左右/盒(約為原研藥的1/30)。
仿製藥在成分上基本和原研藥相同,但由於缺乏大規模臨床驗證,患者在選擇時需謹慎,並建議在專業醫生指導下使用。
五、為什麼價格差異如此巨大?
1.研發成本:原研藥物需經過十年以上研發週期和數億美元投入,因此上市初期定價普遍偏高。
2.醫保准入:國內未納入醫保,意味著患者全額自費,而部分進口藥在美國或歐盟則有保險覆蓋。
3.仿製藥政策差異:部分國家放寬專利保護,允許仿製藥上市,導致價格驟降。
六、佩米替尼在國內的前景與熱點趨勢
1.醫保准入呼聲強烈
隨著更多膽管癌患者使用佩米替尼,患者群體和醫生學界普遍呼籲其盡快納入醫保,以減輕患者經濟負擔。
2.適應症拓展
多項臨床試驗顯示,佩米替尼有望用於:
FGFR突變相關的尿路上皮癌
部分血液系統腫瘤
骨癌及其他實體瘤
3.與免疫治療聯合探索
最新研究正在嘗試將佩米替尼與PD-1/PD-L1免疫檢查點抑製劑聯用,期待進一步提高膽管癌患者的療效。
七、患者最關心的問題匯總
1.療效是否優於化療?
——是的,臨床數據表明佩米替尼的客觀緩解率(36%)遠高於傳統化療(不足10%)。
2.價格是否會下降?
——若未來納入醫保,預計患者實際自付比例會顯著降低;海外仿製藥價格雖低,但需注意渠道正規性與用藥安全性。
3.多久能見效?
——多數患者在用藥2–3個週期(約2–3個月)內能觀察到腫瘤縮小或病情穩定。
4.是否適合所有膽管癌患者?
——僅適用於FGFR2融合或重排陽性的患者,需通過基因檢測確認。
佩米替尼作為全球首個獲批的FGFR抑製劑,填補了膽管癌精準治療的空白,為患者提供了新的治療選擇。雖然當前價格昂貴且未進入醫保,但其突出的療效和可控的安全性,使其成為患者群體高度關注的靶向藥物。隨著未來醫保談判、國產化進展以及仿製藥的發展,佩米替尼的可及性有望逐步提升。
對於患者而言,及時進行基因檢測,確認是否存在FGFR2融合或重排,才能決定是否適合使用佩米替尼。臨床醫生的專業指導和規範治療方案同樣至關重要。
xa0
參考資料
1.《新英格蘭醫學雜誌》:Pemigatinib in Previously Treated, Locally Advanced or Metastatic Cholangiocarcinoma (FIGHT-202 Trial)
2.FDA官網:FDA approves pemigatinib for cholangiocarcinoma with an FGFR2 fusion or rearrangement
3.ASCO 2024會議摘要與相關報導
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
.jpeg)


















