佩米替尼(Pemigatinib)疗效与价格深度解析:从最新热点到患者关切
一、热点引入:肝胆肿瘤新药的聚焦
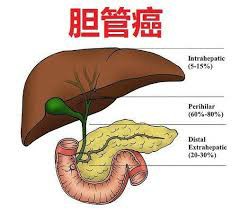
近年来,肿瘤靶向治疗的赛道不断扩展,特别是在胆管癌(Cholangiocarcinoma)等罕见但恶性程度极高的肿瘤领域。2024年,美国临床肿瘤学会(ASCO)会议上,针对FGFR2融合或重排阳性的晚期胆管癌的靶向治疗数据再度成为学界关注的焦点。其中,佩米替尼(Pemigatinib)作为FDA首批批准的针对FGFR2基因异常的口服靶向药,被称为“胆管癌患者的新希望”。
就在今年,多项真实世界研究也在国内外陆续公布,显示佩米替尼在不同线次治疗中均有较好的疗效和耐受性。随着越来越多的患者与医生开始接触这一新药,其疗效与价格也逐渐成为患者群体讨论的热点。
本文将系统解析佩米替尼的临床疗效、适应症拓展进展,并结合国内外价格对比,帮助患者全面了解这款药物。

二、什么是佩米替尼?作用机制解析
佩米替尼(Pemigatinib)是一款口服小分子选择性FGFR抑制剂,主要靶向FGFR1、FGFR2和FGFR3。
1.靶点机制:FGFR基因突变或融合重排会导致细胞信号通路异常激活,促进肿瘤发生发展。佩米替尼通过抑制FGFR的磷酸化过程,阻断其下游信号通路,从而抑制癌细胞的生长和扩散。
2.批准进展:2020年,FDA首次批准佩米替尼用于治疗既往接受过至少一次系统治疗的、存在FGFR2融合或重排的局部晚期或转移性胆管癌患者。这是胆管癌领域首个FGFR靶向药物。
3.研究拓展:目前,佩米替尼还在探索用于骨髓增生异常综合征(MDS)、尿路上皮癌等疾病的可能性,显示出更广泛的临床前景。
三、佩米替尼的临床疗效
在国际多项临床研究中,佩米替尼均展现出较强的疗效。
1.FIGHT-202研究(关键性试验)
入组对象:FGFR2融合或重排阳性的胆管癌患者
主要结果:
客观缓解率(ORR):36%
疾病控制率(DCR):82%
中位无进展生存期(PFS):6.9个月
中位总生存期(OS):21.1个月
结论:相较于传统化疗(ORR不足10%),佩米替尼显著改善了患者的缓解率和生存期。
2.真实世界应用
国内外的多中心临床实践表明,即便在二线或三线用药中,佩米替尼依然能为部分患者带来持久的缓解。
部分患者甚至在用药后肿瘤明显缩小,症状显著改善,生活质量得到提升。
3.安全性
常见副作用包括高磷血症、口腔溃疡、指甲变化、皮疹及轻中度消化道反应。
大多数不良事件为可控和可逆,不会导致严重停药。
四、国内外价格差异与购买渠道
尽管疗效令人期待,但价格始终是患者最关注的现实问题。
1.国内市场情况
佩米替尼已在国内上市,名为“佩米替尼片”。
尚未进入医保目录,因此患者需自费购买。
市场上常见规格:
4.5mg × 14片
9mg × 14片
国内价格区间:2万–5万元/盒(因规格和渠道不同略有差异)。
2.海外市场情况
在美国、欧洲,常见规格为 13.5mg × 14片。
售价:约 7万元人民币/盒(价格随汇率波动)。
3.仿制药选择
以老挝卢修斯制药(Lucius)生产的仿制版为例:
规格:4.5mg × 14片
售价:700元左右/盒(约为原研药的1/30)。
仿制药在成分上基本和原研药相同,但由于缺乏大规模临床验证,患者在选择时需谨慎,并建议在专业医生指导下使用。
五、为什么价格差异如此巨大?
1.研发成本:原研药物需经过十年以上研发周期和数亿美元投入,因此上市初期定价普遍偏高。
2.医保准入:国内未纳入医保,意味着患者全额自费,而部分进口药在美国或欧盟则有保险覆盖。
3.仿制药政策差异:部分国家放宽专利保护,允许仿制药上市,导致价格骤降。
六、佩米替尼在国内的前景与热点趋势
1.医保准入呼声强烈
随着更多胆管癌患者使用佩米替尼,患者群体和医生学界普遍呼吁其尽快纳入医保,以减轻患者经济负担。
2.适应症拓展
多项临床试验显示,佩米替尼有望用于:
FGFR突变相关的尿路上皮癌
部分血液系统肿瘤
骨癌及其他实体瘤
3.与免疫治疗联合探索
最新研究正在尝试将佩米替尼与PD-1/PD-L1免疫检查点抑制剂联用,期待进一步提高胆管癌患者的疗效。
七、患者最关心的问题汇总
1.疗效是否优于化疗?
——是的,临床数据表明佩米替尼的客观缓解率(36%)远高于传统化疗(不足10%)。
2.价格是否会下降?
——若未来纳入医保,预计患者实际自付比例会显著降低;海外仿制药价格虽低,但需注意渠道正规性与用药安全性。
3.多久能见效?
——多数患者在用药2–3个周期(约2–3个月)内能观察到肿瘤缩小或病情稳定。
4.是否适合所有胆管癌患者?
——仅适用于FGFR2融合或重排阳性的患者,需通过基因检测确认。
佩米替尼作为全球首个获批的FGFR抑制剂,填补了胆管癌精准治疗的空白,为患者提供了新的治疗选择。虽然当前价格昂贵且未进入医保,但其突出的疗效和可控的安全性,使其成为患者群体高度关注的靶向药物。随着未来医保谈判、国产化进展以及仿制药的发展,佩米替尼的可及性有望逐步提升。
对于患者而言,及时进行基因检测,确认是否存在FGFR2融合或重排,才能决定是否适合使用佩米替尼。临床医生的专业指导和规范治疗方案同样至关重要。
xa0
参考资料
1.《新英格兰医学杂志》:Pemigatinib in Previously Treated, Locally Advanced or Metastatic Cholangiocarcinoma (FIGHT-202 Trial)
2.FDA官网:FDA approves pemigatinib for cholangiocarcinoma with an FGFR2 fusion or rearrangement
3.ASCO 2024会议摘要与相关报道
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。



















